水に溶けるとイオンになるの違いは何ですか?
「水に溶ける」と「電離する」の違い
水に溶けるという現象は「溶質(イオンや分子)の周りを溶媒分子が囲み、それによって溶質同士が引き離されバラバラになる現象」である。 一方、電離するという現象は「塩を構成する陽イオンと陰イオンが引き離されてバラバラになる現象」である。
キャッシュ
水に溶けてイオンになる物質は?
水に溶かしたとき、その水溶液に電流が流れるようになる物質を 電解質 ( でんかいしつ ) (英語: electrolyte)という。 例) 塩化ナトリウム(食塩)、水酸化ナトリウム、塩化銅、硫酸、塩化水素(塩酸) など。
イオン結合 水に溶けやすい なぜ?
【イオン結晶の水への溶解】
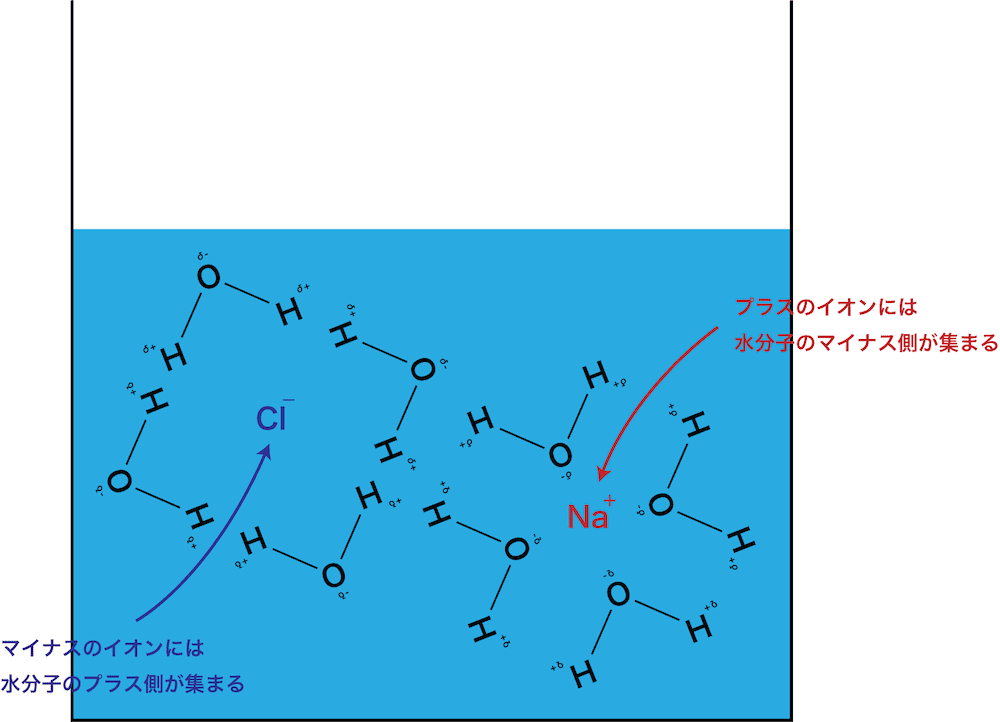
イオン結晶性の物質は,溶液中では陽イオンと陰イオンに電離する。 これらのイオンは極性分子である水分子と静電気力によって緩やかに結合する(左下)。 そのため,イオン結合性のものは水に溶けるものが多い。
キャッシュ
水に溶けるとどうなる?
したがって「溶けるとは,水の力によって,物質が小さくなり,水の中に均一に存在するようになることであり,透明になる。」
キャッシュ類似ページ
金属はなぜイオンになる?
金属は、原子核が電子を引き付ける強さである電気陰性度が弱いため、原子核から電子が離れ、陽イオンになりやすいという性質を持っています。
なぜ金属は溶けるのか?
なぜ金属は溶けるのでしょうか? それは、外から熱が加えられることで金属をつくっていた分子の振動が激しくなり、その場から動き出すからです。 固体(solid)が液体(liqid)になるのです。 この固体と液体の分岐点を融点と言います。
水に溶けて水素イオンを生じる物質は?
酸と塩基 (acid and base)
「酸は、水に溶けると水素イオンH+を生じる物質であり、塩基は、水に溶けると水酸化物イオンOH-を生じる物質である。」
水に溶かすと電離して水素イオンを生じる化合物は?
水に溶かすと水素イオン H+を生じる物質を酸といいます。 H+は水溶液中では水分子H2Oと反応してH3O+として存在しています。 このH3O+をオキソニウムイオンといいます。
なぜイオンになるのか?
原子が電子を失うと、陽子の数が多くなり、原子は+の電気を帯びることになります。 反対に原子が電子を受け取ると、陽子の数より多くなるので、-の電気を帯びることになります。 つまり、電子を失うと陽イオンになり、電子を受け取ると陰イオンになります。 陽イオンになるか陰イオンになるかは、原子の種類で決まっています。
イオン結合と水和の関係は?
一般に,ある化学種(イオン,無機化合物,有機化合物など)が水と結合することをいう. 【Ⅰ】水中に溶解した荷電粒子(イオン,電子)が,そのまわりに1個以上の水分子を強く引きつけ,全体として一つの集団的性質を示すこと.イオンの場合は水和イオン,電子の場合は水和電子という.
電解質とイオンの違いは何ですか?
つまり、物質を水に溶かしたとき、イオンになるものとならないものがあり、電気を通す物質はイオンになるものである。 これを電解質という。
イオンなりやすい なぜ?
金属はどんなイオンになりやすい? そもそもイオンとは、原子が安定な構造をとるために電子をやりとりし、全体として電荷を帯びるようになった粒子のことです。 金属の原子は価電子数が1~3個と少なく、電子(-)を放出して陽イオン(+)になりやすいという性質があります。
銅が塩酸に溶けない理由は何ですか?
・銅は、H2よりイオン化傾向が小さいため塩酸など普通の酸とは反応せず溶けない。 ・希硝酸、濃硝酸、熱濃硫酸(加熱した濃硫酸)は、酸化力のある酸で、一般に銅など銀よりもイオン化傾向の大きい金属を溶かす。
水に溶かすと電離して水酸化物イオンを生じる化合物?
水溶液にしたとき,電離して水酸化物イオンを生じる化合物をアルカリという。
水に溶けると水素イオンを生じる物質は?
「酸は、水に溶けると水素イオンH+を生じる物質であり、塩基は、水に溶けると水酸化物イオンOH-を生じる物質である。」 これをブレンステッドとローリーは水溶液以外にも適用できるように拡張し、「酸とは、水素イオンH+を与える物質であり、塩基とは、水素イオンH+を受け取る物質である。」 と定義した。
イオンになる時のルールは?
原子が陽イオンになるためには、原子核がもつ正電荷による引力を断ち切って、電子が原子の外に出て行く必要があります。 このとき、電子はかなり強いエネルギーをもっていないと、外に出ていくことができません。
イオンとは何なのか?
イオンは原子が電気を帯びた状態のことです。 陽子と中性子を持った原子核と、その周りを飛び回る電子から原子は構成されています。 陽子はプラスの電気を、電子はマイナスの電気を帯びています。 原子核の周りを飛び回る電子は何かの刺激ですぐに原子から出ていったり、入ってきたりするのです。
なぜ水に溶けるのか?
水素原子Hと酸素原子Oの電気陰性度の大小関係は 酸素原子O>水素原子H。 つまり酸素原子が電子を強く引き寄せます。 よって酸素原子は-にかたより、水素原子は+にかたよります。 これが水にものが溶ける原因になります。
水は何で共有結合 なの?
水素原子はその電子軌道に2個、酸素原子は外側の軌道に8個の電子が入った状態になると安定する特別な性質があるため、「共有結合」と呼ばれる水素2個と酸素1個の強い結び付きが起こるのです。
牛乳 何イオン?
カリウムイオンは牛乳乳製品をはじめ、魚介類、野菜類、果物、みそ、しょうゆや肉類などに幅広く含まれており、通常の食生活では不足しない栄養素です。
